Hémopathies malignes du sujet agé : concilier efficacité et tolérance.

Introduction
L’incidence des hémopathies augmente avec l’âge avec un âge médian au diagnostic de 67 ans. Du fait du vieillissement de la population, une nouvelle augmentation de l'incidence et de la prévalence des hémopathies malignes chez les personnes âgées devrait être observée dans les années à venir.
Les taux de survie chez les patients âgés sont généralement inférieurs à ceux des patients plus jeunes. Cette différence est variable selon les hémopathies : plus marquée pour les hémopathies agressives (Leucémie aiguë, lymphome de Burkitt, lymphome B diffus à grandes cellules) et moins marquée pour les lymphomes indolents. Cependant, ces dernières décennies ont été marquées par une amélioration de la survie chez les personnes âgées liée au progrès dans le profilage des hémopathies, ainsi qu’aux thérapeutiques efficaces et ayant un meilleur profil de tolérance pour les sujets âgés (2,3).
Le vieillissement est un processus hétérogène ; l'âge chronologique seul ne suffit pas pour orienter le traitement d’une hémopathie maligne chez le patient âgé. Pour trouver le juste équilibre entre efficacité et tolérance, il faut dépister les critères de fragilité qui correspondent à une diminution des réserves fonctionnelles conduisant à une moins bonne adaptation à un stress aigu. Les décisions doivent tenir compte des caractéristiques de l’hémopathie, de l'âge biologique, des comorbidités, de l'état fonctionnel et de la fragilité, ainsi que les objectifs et souhaits du patient. L’objectif est un maintien de la qualité de vie, de l’autonomie avec préservation des fonctions physiques et cognitives plus que la survie globale (4).
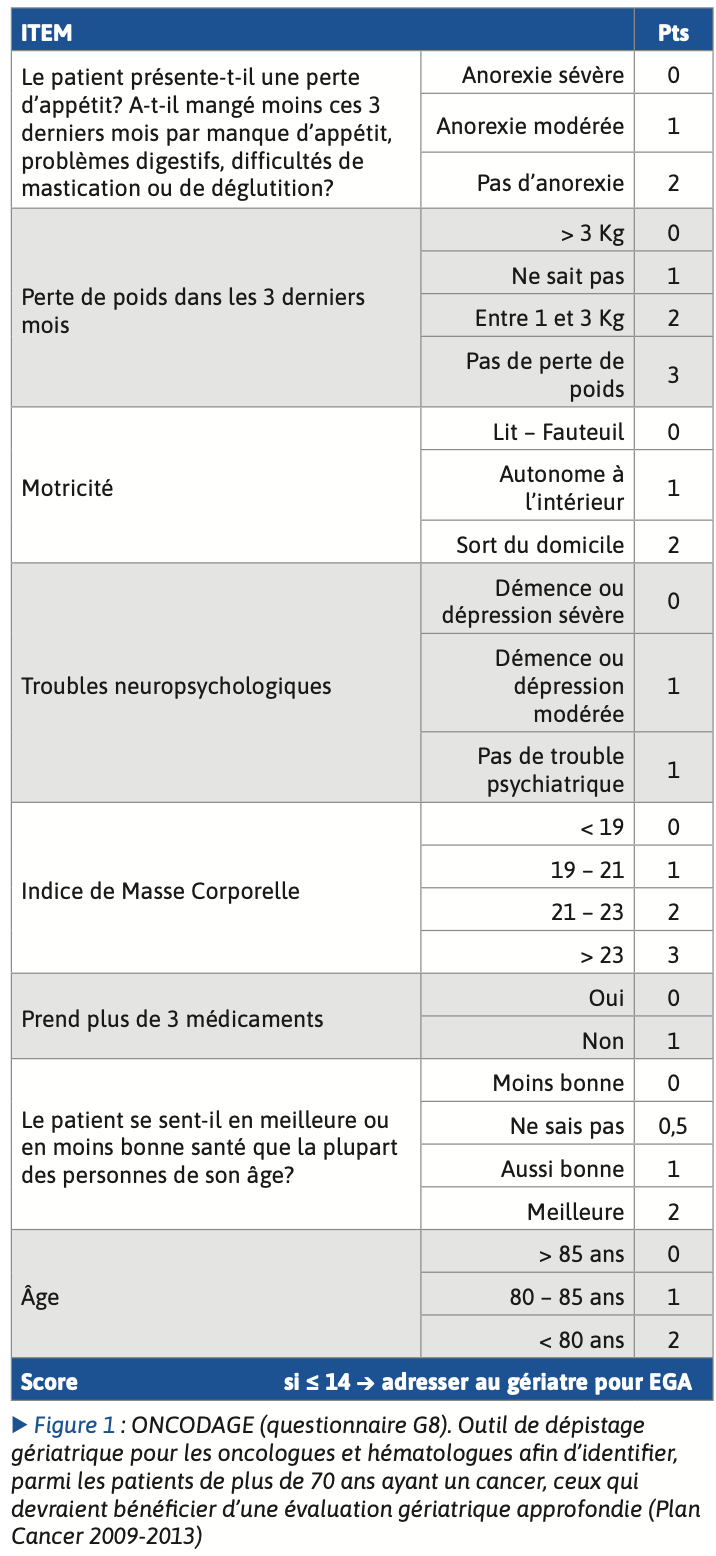
L’Evaluation Gériatrique Approfondie (EGA) est recommandée par les sociétés savantes pour optimiser la prise en charge des patients âgés ayant une hémopathie recevant un traitement systémique. Des outils de dépistage comme le score G8 (5), facilement utilisable en routine, permet aux oncologues ou hématologues d’identifier les sujets de plus de 70 ans atteints de cancer pour lesquels une EGA complète par un gériatre serait bénéfique. L’EGA permet d’identifier les critères de fragilité (dénutrition, perte d’autonomie avec score ADL (6) et IADL (7), trouble de la marche et risque de chute, trouble cognitif, santé mentale, environnement, polymédication, déficit sensoriels) qui sont associés à un risque accru de toxicité, d’arrêt du traitement et de mortalité, même chez les patients en bon état général. L’EGA évalue la réserve fonctionnelle du patient âgé et doit donc orienter l’intensité et les modalités thérapeutiques régulières (8).
De nombreux scores, comme les critères de Fried (9) et l’échelle de Rockwood (10), permettent d’évaluer la fragilité, et donc la réserve fonctionnelle d’un patient âgé. Certains sont spécifiques d’une hémopathie, comme le score de fragilité IMWG (11) dans le myélome. L’évaluation gériatrique approfondie permet cette stratification et surtout d’identifier les facteurs de fragilité à prendre en charge tout au long de l’hémopathie.
Ces différentes approches permettent d’identifier en pratique 3 groupes de patient âgé de plus de 70 ans : « en forme/robuste/fit », « intermédiaire/vulnérable/unfit », « fragile/frail ».
Il existe encore des lacunes importantes dans les données disponibles concernant l’efficacité et la tolérance des traitements chez les patients âgés et fragiles, qui sont souvent exclus des essais cliniques ou sous représentés (12).
Stratégies spécifiques des principales hémopathies malignes
Chaque hémopathie a ses propres particularités dans la réflexion pré-thérapeutique chez le sujet âgé : une adaptation des protocoles de chimiothérapie (rythme, dose, voies d’administration…), des thérapies orales moins contraignantes avec de meilleurs profils de tolérance en évitant les hospitalisations répétées, ou encore des stratégies palliatives actives permettant de ralentir l’évolution de la maladie et les complications invalidantes de l’hémopathie (dépendance transfusionnelle, douleurs, asthénie).
Leucémie myéloïde aiguë (LAM)
Les LAM du sujet âgé sont souvent de mauvais pronostic (caryotypes complexes). Le profilage cytogénétique et moléculaire est donc important pour guider la stratégie thérapeutique. La chimiothérapie intensive (7+3) est à discuter chez les patients de moins de 70 ans sans aucun critère de fragilité ayant une LAM de risque favorable ou intermédiaire, tandis que le CPX-351 est préféré pour les formes de mauvais pronostic ou secondaires (13). L'allogreffe à conditionnement réduit reste marginale, réservée aux patients jusqu'à 70 ans sans comorbidité ni critère de fragilité. Pour les patients inéligibles au traitement intensif, l'association Vénétoclax® avec agent hypométhylant (Azacitidine ou Decitabine) ou Cytarabine faible dose permet d’obtenir 65 % de rémission complète composite et une survie médiane de 15 mois avec une bonne tolérance chez les sujets âgés (14). L'Azacitidine peut être réduite à 5 jours selon la tolérance (notamment en cas de cytopénie) (15). Les inhibiteurs d'IDH selon le profil mutationnel sont des traitements relativement bien tolérés chez le sujet âgé (16).
Leucémie aiguë lymphoïde (LAL)
Les LAL du sujet âgé sont elles aussi de plus mauvais pronostic (davantage d'anomalies cytogénétiques, de mutations TP53, de transcrit BCR : ABL) participant à une survie historiquement inférieure à 20 % avec les chimiothérapies conventionnelles. Pour les LAL Phi-, les schémas de référence actuels chez le patient âgé combinent le blinatumomab et l’inotuzumab à la corticothérapie +/- chimiothérapie permettant 90-100 % de rémission complète avec une survie globale de 46-73 % à 3-5 ans avec une meilleure tolérance que la chimiothérapie conventionnelle. Pour les LAL Phi+, les inhibiteurs de tyrosine kinase (ponatinib, imatinib) associés à une chimiothérapie de faible intensité permettent d’obtenir un taux de rémission après induction > 90 % avec des taux de survie sans progression entre 8 et 20 mois selon les molécules (17).
Lymphome B diffus à grandes cellules
Pour la prise en charge de première ligne, les patients âgés robustes doivent recevoir le traitement standard R-CHOP (rituximab, cyclophosphamide, doxorubicine, vincristine, prednisone) avec la même efficacité que chez le sujet jeune. Chez les patients intermédiaires, ou de plus de 80 ans les schémas thérapeutiques à dose réduite tels que le R-miniCHOP ou le R-miniCEOP sont préférables. La dose de corticoïdes peut être adaptée dans certains cas selon le terrain et la tolérance. La radiothérapie peut être proposée sur les formes localisées. En cas de progression ou de rechute un traitement par CAR T-cells peut être proposé aux patients « fit ». Les anticorps bi spécifiques sont à proposer chez les patients non éligibles aux CAR T-cells ou les refusant (18–20). Ils peuvent être associés à de la chimiothérapie selon les comorbidités et critères de fragilité du patient, pour augmenter la survie sans progression. L’association Glofit-Gemox associant le GLOFITAMAB® à une chimiothérapie par Gemcitabine + Oxaliplatine obtient de très bons résultats avec une médiane de survie sans progression de 13.8 mois (21).
Lymphome de Hodgkin
Le pronostic du lymphome de Hodgkin chez le patient âgé est nettement plus défavorable que chez le sujet jeune. Le traitement de référence chez les sujet âgés éligibles à un traitement est un protocole de chimiothérapie de type AVD (sans bléomycine) avec si possible adjonction d’un anti PDL1 de type Nivolumab® qui présente un bon profil de tolérance (22).
Myélome multiple
Le myélome est une hémopathie principalement du sujet âgé. Le score R-ISS (albumine, LDH, bêta 2 microglobuline et anomalies cytogénétiques (del(17p), t(4;14), t(14;16)) ainsi que la mutation TP 53 restent pronostiques chez les personnes âgées et doivent être pris en compte dans le choix du traitement initial.(23)
En première ligne thérapeutique, la quadrithérapie par Daratumumab, Bortezomid, Lenalidomide et Déxaméthasone(24) reste le protocole de référence chez le sujet de moins de 80 ans robuste. L’autogreffe n’est indiquée qu’en cas de risque défavorable chez les patients < 70 ans sans aucune comorbidité ni critère de fragilité. Les possibilités d’adaptation de traitements de premières lignes sont un tri thérapie par Daratumumab + Lénalidomine + Déxaméthasone (DRD) pour les patients « intermediaires ou fragile » (25), voire Lénalidomide + Dexaméthasone (Rd) pour les patients très fragiles. La posologie de Lénalidomide peut être diminuée selon la toxicité (notamment cytopénie, asthénie, troubles digestifs).
Lors d’une rechute avec indication théorique à un traitement par CAR-t cells leur utilisation doit être discutée après évaluation gériatrique même après 80 ans devant une efficacité majeure et un profil de tolérance satisfaisant chez les patients bien sélectionnés (cf infra). Lorsqu’un patient est inéligible ou refuse les CAR-t cells il faut envisager un traitement par anticorps bi spéciques, systématiquement associé à une supplémentation en immunoglobulines (Ig) intraveineuses. Seuls les patients très fragiles ne sont pas éligibles aux anticorps bispécifiques sur le plan gériatrique.
La dose et la durée des corticoïdes sont adaptsé selon les situations afin de réduire sa toxicité chez les sujets âgés. Selon les recommandations de l’intergroupe français du myélome (IFM), chez les patients « fit » traités Dara-VRD, la dexaméthasone doit être réduite à 20mg pour les sujets de plus de 70 ans et arrêtée lors de l’entretien par daratumumab et lenalidomide. Chez les sujets âgés traités par DRD, elle doit être arrêtée à partir du 6e cycle chez les moins de 75 ans et à partir du 2e cycle pour les plus de 75 ans(26).
Lors d’un traitement par Teclistamab® les corticoïdes sont administrés au premier cycle uniquement.
Les syndromes myélodysplasique (SMD)
Les SMD présentent une grande hétérogénéité clinique et moléculaire, caractérisée par des cytopénies variables (27).
La prise en charge repose sur la stratification IPSS/IPSS-R et le profilage moléculaire.
Dans les formes à faible risque, l’objectif est le contrôle des symptômes et la réduction de la dépendance transfusionnelle. Les agents stimulant l'érythropoïèse sont utilisés en première intention (EPO). Après échec d’EPO, l’indépendance transfusionnelle peut être obtenue par le Luspatercept en cas de SMD avec sidéroblastes en couronne, et par le lénalidomide pour les délétions 5q, même chez les sujets âgés fragiles. Dans les formes à haut risque, les agents hypométhylants, tels que l’azacitidine ou la décitabine, constituent le traitement de première ligne pour retarder la transformation en leucémie aiguë et diminuer les besoins transfusionnels. L’allogreffe de cellules souches reste la seule option curative, mais est rarement envisageable chez les patients âgés (28).
Focus CAR-t cells et anticorps bi spécifiques
Les CAR t-cells ont démontré une efficacité comparable aux sujets jeunes (réponse complète, survie sans progression et survie globale), chez les personnes âgés ≥ 70 ans atteintes d'hémopathies malignes, en particulier dans les cas de lymphome diffus à grandes cellules B (LDGCB) récidivant/réfractaire, de lymphome folliculaire et de myélome multiple. Leur efficacité est la même chez le sujet âgé que chez les adultes plus jeunes. Dans le DLBCL, les CAR t-cells permettent d'obtenir des taux de réponse complète plus élevés et une survie sans progression plus longue par rapport aux anticorps bispécifiques. Quel que soit la pathologie les taux de CRS et d’ICANS (neurotoxicité) de grade 3 sont plus élevés que chez les jeunes (jusqu’à 15 %). Ces complications augmentent le risque de complications gériatriques avec notamment une perte d’autonomie et de qualité de vie post hospitalisation(29) (30) (31).
Concernant les anticorps bi spécifiques, les patients âgés bénéficient d’une même efficacité que les sujets jeunes. Ils sont très bien tolérés. Les taux de CRS, neurotoxicité et cytopénies grade 3 sont faibles. Le principal risque reste l’immunodépression profonde avec un risque infectieux majeur, notamment d’infections opportunistes graves (32). Il faut donc penser à espacer les injections dès que la réponse est obtenue (notamment dans le myélome).
Soins de support : du diagnostic à la fin de la prise en charge
Les soins de support sont essentiels pour réduire la toxicité des traitements, préserver la qualité de vie et maintenir l'autonomie chez les sujets âgé atteints d’hémopathie maligne (33). L'éducation sur les effets secondaires renforce l'autonomie et favorise l'observance et la détection précoce des événements indésirables. Les soins de support englobent plusieurs dimensions qui doivent être réévaluées tout au long de la prise en charge : nutrition, état neuropsychologique, état fonctionnel, comorbidités, ostéoporose, cytopénies, iatrogénie et polymédication, contexte socio-environnemental (34).
La prévention des effets indésirables des traitements est primordiale, notamment dans un contexte de polymédication fréquente chez le sujet âgé. Ils peuvent être liés aux traitements de l’hémopathie (neuropathie, sécheresses cutanées, l’asthénie et troubles digestifs...) ou à la polymédication (inobservance, troubles de la déglutition, interactions médicamenteuses…), ou encore aux traitements associés.
Certains médicaments fréquemment administrés majorent le risque de confusion et de chute (acupan, tramadol, anti histaminiques H1, métoclopramide, benzodiazépine, antibiotiques, morphiniques, corticoïdes…). La constipation est fréquente chez le sujet âgé avec un risque de fécalome et d’occlusion. Elle est favorisée par l’immobilité et certains traitements (vincristine, odansetron, morphine…). L'ordonnance unique, les passages infirmiers ou la réalisation de piluliers hebdomadaires optimisent l'observance.
Les corticoïdes, fréquemment utilisés en hématologie, génèrent des effets indésirables majeurs chez le sujet âgé : infections, sarcopénie, déminéralisation osseuse, déséquilibre de diabète, hypertension et confusion. Le choix de la molécule, sa posologie et la durée de traitement doivent être réévalués régulièrement avec une réduction ou un arrêt dès que possible pour limiter la morbi-mortalité.
La prophylaxie anti-infectieuse repose sur la vaccination systématique : pneumocoque, zona, ainsi que grippe et covid saisonniers. Les prophylaxies anti infectieuses habituelles ne doivent pas être négligées (cotrimoxazole, valaciclovir, amoxicilline, posaconazole selon les hémopathies). La supplémentation en Ig IV doit être systématique chez les patients traités par anticorps bi spécifique pour un myélome, et doit être discutée selon les épisodes infectieux pour les autres hémopathies.
L’activité physique avec kinésithérapie ou activité physique adaptée si nécessaire, ainsi que le dépistage et prise en charge de la dénutrition, de la sarcopénie, de la neuropathie réduisent le risque de chutes et de perte fonctionnelle. S'y associent la prise en charge de la santé osseuse (biphosphonates, calcium, vitamine D notamment dans le myélome). L’adaptation des aides selon les besoins permet un maintien à domicile le plus long possible.
La douleur (aiguë comme chronique) génère anxiété, dépression, perte d'autonomie et confusion. Son dépistage régulier est essentiel. Il existe des thérapeutiques non médicamenteuses (hypnose, aromathérapie, acupuncture, TENS…) et des traitements médicamenteux qui doivent être adaptés à l'âge (contre-indication aux AINS). La radiothérapie locale antalgique est envisageable en situation palliative ou en cas de lymphome localisé. Les centres antidouleurs sont un recours très utile.
Le dépistage des troubles neurocognitifs est crucial car ils ont une valeur pronostique indépendante et majorent le risque confusionnel. La confusion augmente le taux d’hospitalisations, la perte d'autonomie et l’arrêt des traitements. Les troubles thymiques, fréquents dans cette population, impactent significativement la qualité de vie et nécessitent une prise en charge adaptée, médicamenteuse ou non.
Eviter la dépendance iatrogène
La dépendance iatrogène liée à l'hospitalisation chez les patients âgés désigne la perte d'autonomie nouvelle ou aggravée dans les activités de la vie quotidienne qui survient comme conséquence directe des soins médicaux ou de l'environnement hospitalier. Elle est fréquente chez les personnes âgées hospitalisés (30 à 60 %). La dépendance qui en résulte peut persister pendant des mois ou devenir permanente, augmentant ainsi le risque d'institutionnalisation et de mortalité.
La plupart des cas de dépendance iatrogène peuvent être évités grâce à des interventions ciblées. La sensibilisation et la formation des équipes médicales et paramédicales est la pièce angulaire de la réduction de ces risques et l’optimisation de la prise en charge (figure 1).
Lorsque le patient est âgé, polymorbide et/ou présente des risques ou complications gériatriques, faire appel à l’équipe mobile de gériatrie ou une hospitalisation en service de gériatrie peut permettre d’optimiser cette prise en charge globale.
La meilleure option est de réserver l’hospitalisation aux cas indispensables. Et lorsqu’elle est indispensable elle doit être la plus courte possible. Afin d’éviter les hospitalisations et passages aux urgences, la prise en charge ambulatoire et le lien ville-hôpital doit être optimisé. La mise en place d’aides à domicile doit être anticipée et adaptée. Les infirmier.es de coordination restent un lien majeur pour rester en contact avec le patient, son entourage et/ou les aides professionnelles afin d’identifier précocement une problématique qui pourrait être prise en charge en ambulatoire avant une dégradation qui nécessitera une hospitalisation.
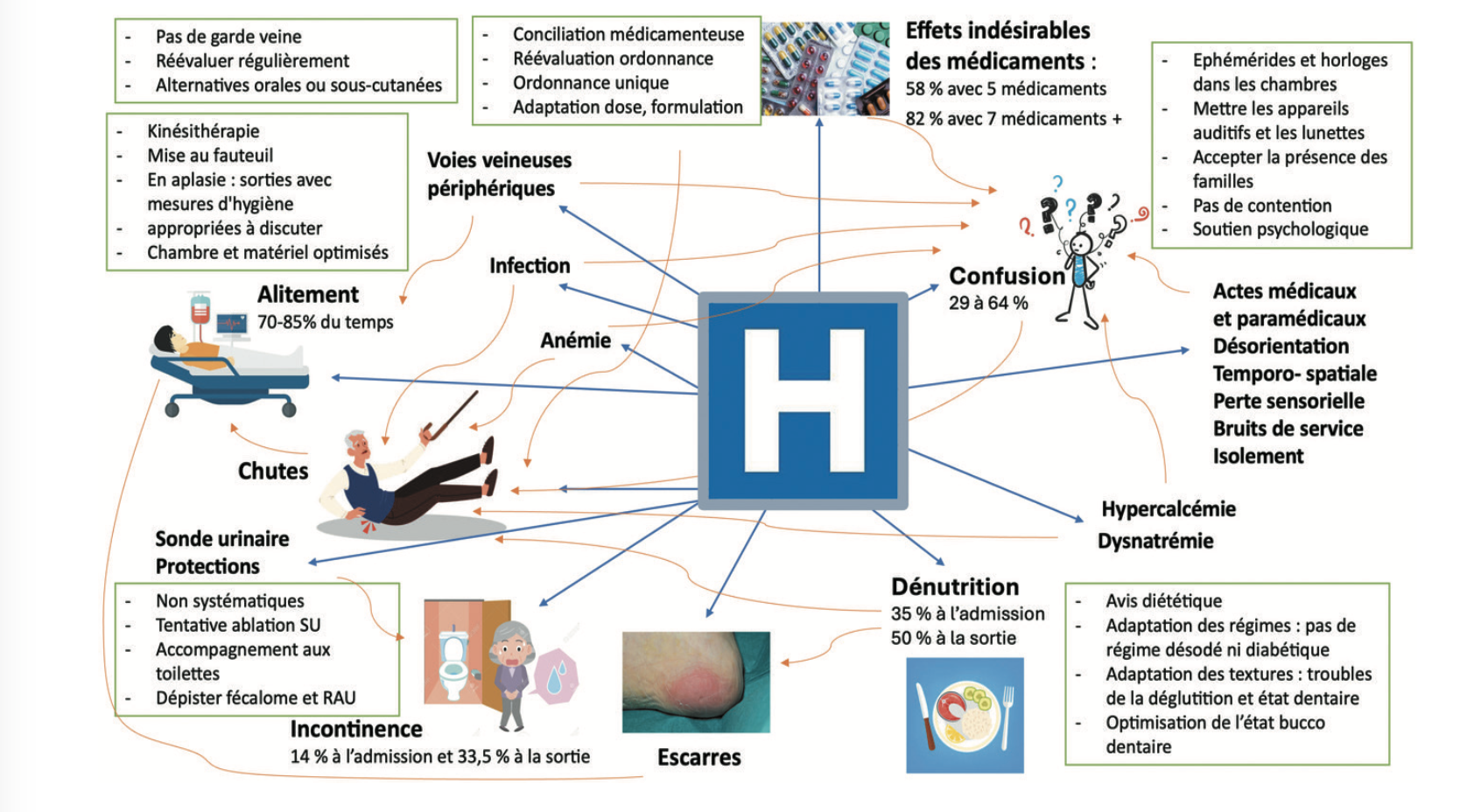
Figure 2 : La dépendance iatrogène liée à l’hospitalisation : comment éviter la cascade gériatrique ? (Non exhaustif)
SU : sonde urinaire. RAU : rétention aiguë d’urine
Conclusion
L’approche visant à équilibrer l'efficacité et la tolérance des traitements chez les patients âgés atteints d’hémopathie maligne repose sur une évaluation multidimensionnelle (caractéristiques de l’hémopathie, âge chronologique, comorbidités, critères de fragilités). L’objectif est triple : ne pas sous-traiter des sujets âgés en raison de leur âge chronologique lorsqu’ils ont une bonne réserve fonctionnelle; ne pas priver des patients âgés vulnérables mais éligibles à des thérapeutiques adaptées à leur profil (qu’ils soient curatifs ou palliatif actif) ; mais également savoir ne proposer que des soins de supports exclusifs dans certains cas.
Tout au long de la prise en charge il est nécessaire de réévaluer le rapport efficacité/tolérance ainsi que l’avis et les souhaits du patient. Les facteurs de fragilités, les comorbidités et les difficultés socio-environnementales doivent être dépistées et prises en charge pendant toute la durée du suivi. La réalisation des scores ADL et IADL au diagnostic, pendant les traitements, avant et après hospitalisation permettent de surveiller l’autonomie des patients et anticiper la mise en place d’aides et d’identifier facilement l’apparition de fragilité. Les soins de supports doivent être systématiques en parallèle du traitement.
Cette approche multidimensionnelle repose donc sur une collaboration rapprochée entre hématologue, gériatre, soins de supports, infimier.e.s, intervenants ambulatoires dès le diagnostic et jusqu’à la fin de la prise en charge afin d’optimiser la survie avec la meilleure qualité de vie possible.

