Résumé
L’atteinte rénale au cours des vascularites à ANCA est fréquente et aggrave le pronostic à long terme. La dissection des mécanismes physiopathologiques mis en jeu au cours des vascularites à ANCA a permis d’améliorer nos outils diagnostiques et thérapeutiques. La biopsie rénale reste incontournable et permet de préciser le pronostic à long terme. A moyen terme, elle sera complétée par des biomarqueurs non invasifs qui guideront le clinicien dans le choix de traitements personnalisés.
Introduction
Les vascularites systémiques représentent un ensemble hétérogène de maladies caractérisées par une atteinte inflammatoire de la paroi vasculaire artérielle et/ou veineuse. La sténose ou l'occlusion de la lumière vasculaire par une thrombose ou une prolifération intimale est à l’origine des manifestations cliniques. Depuis 1994, les différents types de vascularites systémiques sont individualisés au sein de la nomenclature de Chapel Hill, en fonction du calibre des vaisseaux atteints et de la nature de l’infiltrat inflammatoire1.
Les vascularites associées aux ANCA (anticorps anti cytoplasme de polynucléaires nneutrophiles) (VAA) représentent un groupe de maladies défini par une vascularite nécrosante touchant les vaisseaux de petit calibre (artérioles, capillaires et/ou veinules) et associé à la présence d’ANCA dirigés contre la Myélopéroxidase (ANCA anti-MPO) ou contre la Protéinase 3 (ANCA anti-PR3), selon la nomenclature de Chapel Hill actualisée en 2012. L’atteinte rénale est fréquente au cours des VAA, présente chez 50 à 90 % des patients, plus fréquente et plus sévère en présence d’ANCA anti-MPO2. Au cours des dix dernières années, l’amélioration des connaissances physiopathologiques a permis d’accroître notre outil diagnostique et thérapeutique.
Dans ce numéro, nous résumerons la vision actuelle de la physiopathologie des VAA puis nous préciserons les nouveautés diagnostiques, pronostiques et thérapeutiques qui en découlent.
Physiopathologie des vascularites à ANCA
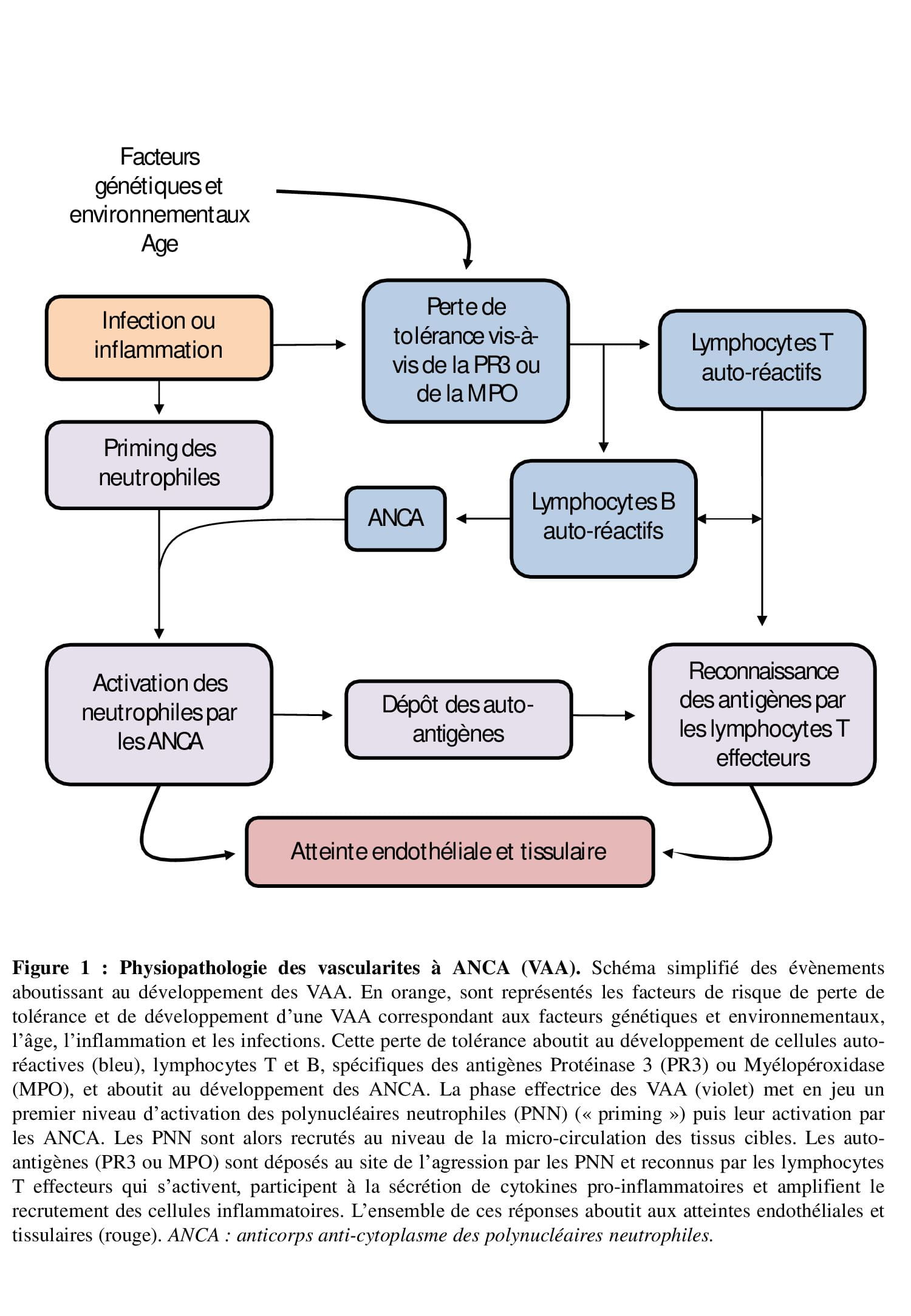
La Figure 1 résume la physiopathologie des VAA. Les facteurs prédisposant au développement d’une VAA sont mixtes. Il existe des facteurs génétiques : ANCA anti-PR3 associés à l’allèle HLA-DPB1*04 :01 et aux gènes codant l’α1-antitrypsine (SERPINA1), et la PR3 (PRTN3)3 ou ANCA anti-MPO associés au sous-type HLA-DQ. Des facteurs environnementaux tels que l’exposition aux silices, à la pollution ou à des toxiques tels que le levamisole contenu dans la cocaïne. Enfin, il existe des facteurs infectieux tels que le portage chronique nasal du Staphylocoque Aureus. Sur ce terrain plus ou moins prédisposé, se produit une perte de tolérance vis-à-vis d’un antigène du soi, PR3 et/ou MPO, aboutissant au développement d’ANCA. À l’état basal, les PNN n’expriment pas ces antigènes à leur surface. Cependant, après un premier signal d’activation (ou « priming ») pouvant correspondre à une infection ou à un toxique, les PNN expriment ces autoantigènes à leur surface, permettant leur liaison aux ANCA. Celle-ci induit une activation robuste des PNN qui deviennent capables d’adhérer à l’endothélium vasculaire. La dégranulation de leur contenu intra-cellulaire libère de nombreuses espèces réactives de l’oxygène et protéases. De plus, les PNN activés peuvent être soumis à un type particulier de mort cellulaire, dénommée « NETOSE » au cours de laquelle ils libèrent des « Neutrophil Extra-cellular TRAPS »4. Ces derniers correspondent à des filaments de chromatine décondensée, capables d’induire une lésion endothéliale directe et de transférer les antigènes MPO ou PR3 vers l’endothélium et les cellules dendritiques. Enfin, la libération de nombreuses chimiokines et le dépôt d’auto-antigènes participent au recrutement de lymphocytes T auto-réactifs et de monocytes, qui aggravent l’atteinte cellulaire. Les modèles murins ont également permis de mettre en évidence un rôle important du système du complément. En effet, les PNN activés sont capables de libérer l’anaphylatoxine C5a. Ce puissant médiateur inflammatoire amplifie le recrutement des cellules immunitaires sur le lieu de l’inflammation, favorise la rétention des PNN dans la micro-circulation et l’interaction entre les cellules dendritiques présentant les auto-antigènes. Enfin, les monocytes et macrophages peuvent également être activés par les ANCA et jouent un rôle important notamment par leur effet pro-fibrotique responsable des lésions chroniques.
Nouveautés diagnostiques et pronostiques dans l’atteinte rénale des VAA
Sur le plan rénal, le diagnostic repose sur la mise en évidence d’un syndrome de glomérulonéphrite rapidement progressive mais ne doit pas être méconnu en cas de présentation plus insidieuse, en particulier dans les formes associées aux anticorps anti-MPO. Le diagnostic sérologique repose sur l’identification d’ANCA anti PR3 et/ou MPO par technique ELISA, plus sensible que l’immunofluorescence indirecte. La persistance des ANCA au cours du traitement et leur réapparition sont des facteurs de risques de rechute5 tandis que leur négativation est associée à une survie sans récidive plus longue6.
À l’heure actuelle, la biopsie rénale reste indispensable en cas de mise en évidence d’une insuffisance rénale et/ou d’une protéinurie et/ou d’une hématurie, à visée diagnostique et pronostique.
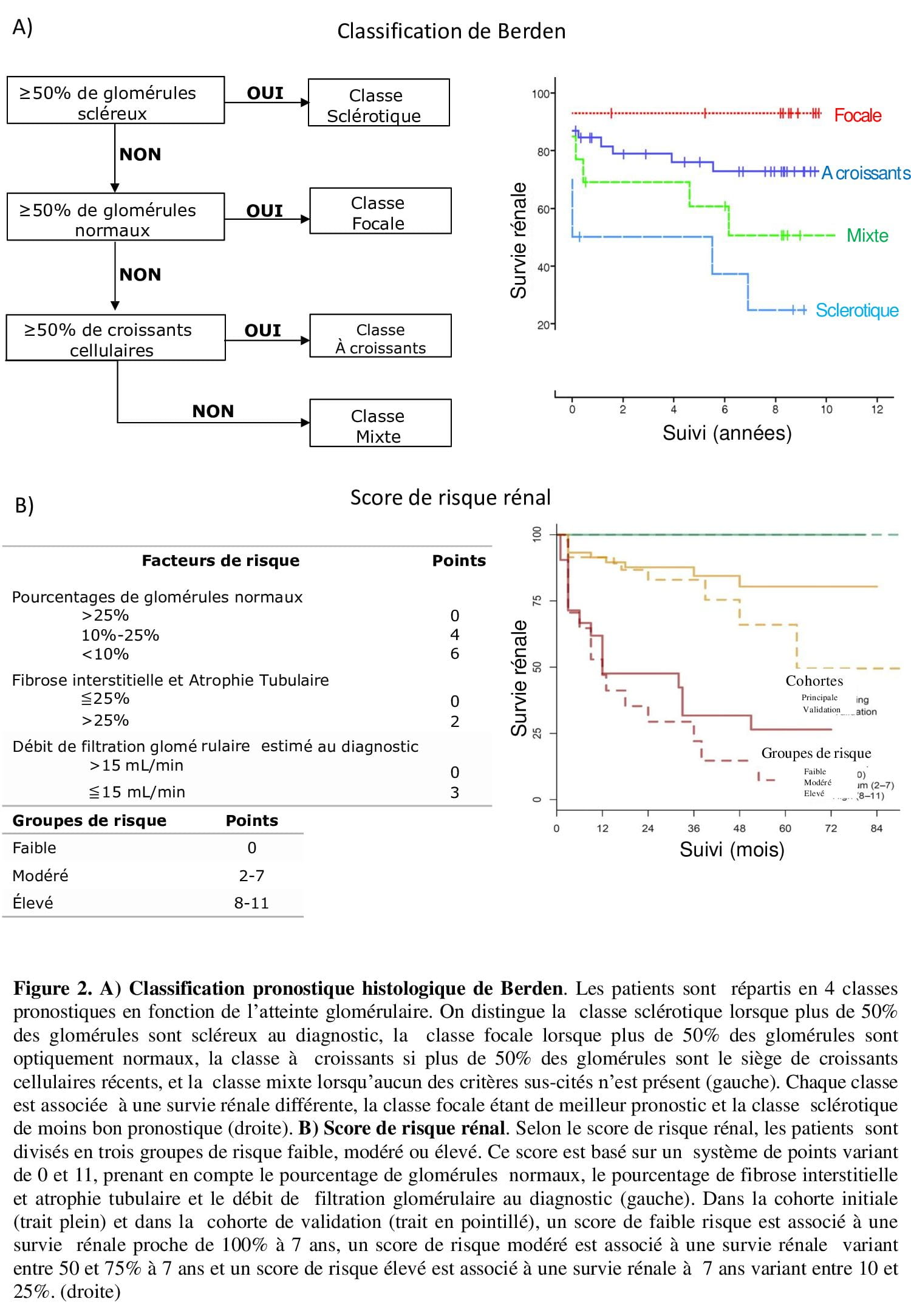
La première classification pronostique rénale, proposée en 2010 par Bajema et al, reposait exclusivement sur l’atteinte glomérulaire (Figure 2A)7. Cette classification a été évaluée dans de multiples cohortes indépendantes8. Cependant, l’utilisation de cette classification histologique n’améliorait pas la prédiction du risque d’insuffisance rénale terminale (IRT) en analyse multivariée9. En 2018, l’équipe de Brix et al. a proposé pour la première fois un score clinico-pathologique prenant en compte l’atteinte glomérulaire, l’atteinte tubulo-interstitielle et le débit de filtration glomérulaire au diagnostic10. Ce score de risque rénal (SRR ; ANCA Renal Risk Score en anglais) divise les patients en trois groupes :
■ Les patients de risque faible, dont la survie rénale à 5 ans est proche de 100 % ;
■ Les patients de risque élevé dont la survie rénale est de l’ordre de 25 % à 5 ans ;
■ Les patients de risque intermédiaire (Figure 2B).
L’étude initiale et les cohortes de validations récemment publiées semblent en faveur d’une discrimination pronostique supérieure du SRR en comparaison à la classification de Berden10. De même, notre équipe a récemment validé et confirmé la supériorité de ce score pronostic et propose l’ajout d’un item étudiant la présence ou non d’une artérite des petites artères rénales au diagnostic11.
À l’heure actuelle, se développe des biomarqueurs non invasifs dans le but de prédire le risque de rechute et, à terme, de guider le clinicien dans le choix des traitements12. Parmi les plus prometteurs, les fragments d’activation du complément retrouvés dans les urines (Bb, C3a, C5a et sC5b-9) sont augmentés en cas d’activité de la VAA et inversement corrélés au nombre de glomérules normaux. Plusieurs études rétrospectives ont également démontré l’association entre un taux sérique bas de la fraction C3 du complément et un pronostic rénal plus sombre. Avec le développement d’inhibiteurs du complément dans le traitement des VAA, ces biomarqueurs permettront probablement de guider le choix des traitements. Le CD163 soluble urinaire semble également être un biomarqueur non invasif prometteur. La concentration urinaire de ce marqueur macrophagique est associé à l’activité des VAA. Récemment, Moran et al. ont démontré, en vie réelle, une élévation de ce biomarqueur en cas de poussée de VAA et sa diminution en rémission. Ils ont, par ailleurs, proposé un seuil normalisé sur le taux de protéinurie qui pourrait permettre une utilisation en routine13.
Nouveautés thérapeutiques
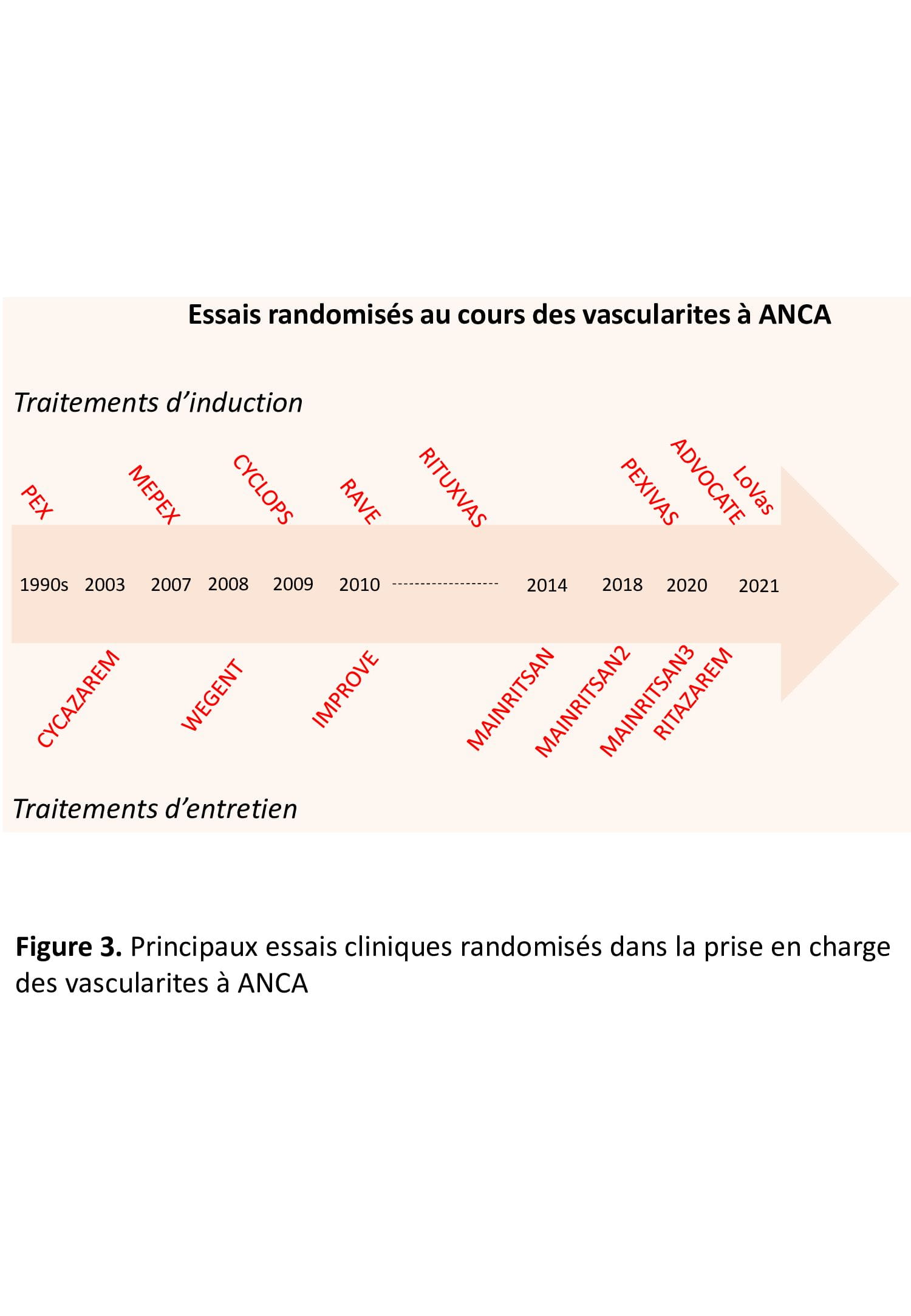
Le traitement des VAA à beaucoup évolué au cours des 20 dernières années, grâce à de multiples essais randomisés concernant le traitement d’induction14-20 et le traitement d’entretien (Figure 3)21-25.
La prise en charge actuelle d’une VAA avec atteinte rénale repose sur la mise en place en urgence d’un traitement d’induction. Ce traitement consiste en l’administration de bolus de corticoïdes à forte dose par voie intraveineuse associé à un traitement immunosuppresseur soit par CYCLOPHOSPHAMIDE soit par RITUXIMAB. Deux essais cliniques randomisés ont prouvé la non-infériorité du RITUXIMAB comparé à la CYCLOPHOSPHAMIDE pour la mise en rémission des patients. Cependant, les patients présentant une atteinte rénale sévère (créatinine supérieure à 350 mol/L) étaient exclus de ces essais. Actuellement, le traitement par CYCLOPHOSPHAMIDE est souvent préféré au RITUXIMAB en cas d’atteinte rénale sévère, dans l’hypothèse d’un effet plus rapide. Récemment, une étude rétrospective portant sur 467 patients dont 251 avec atteinte rénale sévère (définie par un DFG inférieur à 30 mL/min) au diagnostic d’une VAA, ne retrouvait pas de différence significative entre les deux traitements concernant la mise en rémission, le risque d’insuffisance rénale terminale et de décès. Seul un essai clinique randomisé permettra de répondre définitivement à cette question. Jusqu’à récemment, la prise en charge d’une VAA avec atteinte rénale sévère nécessitait l’initiation d’échanges plasmatiques en urgence. Cependant, l’étude PEXIVAS, plus grand essai randomisé jamais réalisé en néphrologie, a récemment démontré l’absence d’efficacité de ce traitement, dont l’indication pourrait être amenée à disparaitre.
Après obtention de la rémission, la prévention de la récidive de la maladie est assurée par le traitement d’entretien. Depuis les résultats des essais MAINRITSAN et RITAZAREM, le traitement d’entretien des VAA repose sur le RITUXIMAB, supérieur au traitement par AZATHIOPRINE.
Enfin, l’effort actuel consiste à minimiser le plus possible la dose et la durée d’administration des corticoïdes afin de limiter les effets secondaires. Par exemple, l’essai clinique CORTAGE a démontré la possibilité de réduire la dose et la durée de la corticothérapie dans une population âgée de plus de 65 ans.
Plus récemment, l’étude PEXIVAS a démontré la non-infériorité d’une dose réduite de corticoïdes. Enfin, une étude récemment publiée dans JAMA propose une décroissance encore plus rapide des corticoïdes, non inférieure au protocole « low-dose » de l’étude PEXIVAS, mais excluant les patients dont le DFG est inférieur à 40 mL/min/1,73 m2.
De nouveaux traitements sont en cours d’évaluation. Le plus proche d’aboutir en pratique clinique est l’AVACOPAN, un inhibiteur soluble du récepteur de C5a. L’essai de phase IIIa, ADVOCATE, a démontré la non-infériorité de l’AVACOPAN en comparaison au régime standard par corticoïdes à 26 semaines, une épargne cortisonique importante et une réduction des effets indésirables. Son coût risque néanmoins d’être un frein initial à l’utilisation. De plus, de nombreux essais sont en cours :
■ Ciblant les lymphocytes B : l’essai COMBIVAS (NCT03967925) compare actuellement l’ajout du Beblimumab au traitement standard (chez les patients ayant une clairance supérieure à 30 mL/min) et l’essai ENDURRANCCE (NCT0394287) un régime à base de rituximab et cyclophosphamide faible dose à un traitement d’induction standard par rituximab et coticoïdes.
■ Ciblant les lymphocytes T, l’essai ALEVIATE (NCT01405807) étudie l’apport de l’Alemtuzumab (anti-CD52) en traitement d’induction et l’essai ABROGATE (nct02108860) l’Abatacept, toujours en traitement d’induction.
■ Ciblant le complément, l’essai INFLARX (NCT03895801) étudie un inhibiteur direct du C5a (vilobelimab, IFX-1) actuellement en phase II.
Enfin, l’essai randomisé RENATO, étudiant l’efficacité de la Pioglitazone (agoniste sélectif des récepteurs nucléaires PPAR-gamma) dans l’induction d’une tolérance rénale aux VAA, débutera en France sous la direction du Pr Karras à la fin de l’année 2021.
En somme, l’objectif actuel est d’individualiser au maximum le traitement des patients porteurs d’une VAA et d’éviter tout risque de « sur-traitement ». En effet, la prise en charge ayant radicalement amélioré le pronostic des patients, l’enjeu actuel est de diminuer les complications infectieuses et tumorales, directement liées à l’immunodépression.
Conclusion
Une meilleure compréhension de la physiopathologie des VAA amène progressivement au développement de nouveaux outils diagnostiques, pronostiques et thérapeutiques, illustrant parfaitement l’importance de la recherche translationnelle et l’évolution progressive vers une médecine personnalisée.
Mots clés vascularites à ANCA, insuffisance rénale aiguë, biopsie rénale, biomarqueurs non invasifs, médecine personnalisée.
Liens d’intérêt L’auteur n’a pas précisé au moment ou nous « bouclions » ce numéro ses éventuels liens d’intérêts.
Date de l'article : Décembre 2021
References
1. Jennette JC, Falk RJ, Bacon PA, Basu N, Cid MC, Ferrario F, et al. 2012 revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. Arthritis and rheumatism. 2013;65(1):1-11.
2. Franssen C, Gans R, Kallenberg C, Hageluken C, Hoorntje S. Disease spectrum of patients with antineutrophil cytoplasmic autoantibodies of defined specificity: distinct differences between patients with anti-proteinase 3 and anti-myeloperoxidase autoantibodies. Journal of internal medicine. 1998;244(3):209-16.
3. Jagiello P, Gencik M, Arning L, Wieczorek S, Kunstmann E, Csernok E, et al. New genomic region for Wegener's granulomatosis as revealed by an extended association screen with 202 apoptosis-related genes. Human genetics. 2004;114(5):468-77.
4. Kessenbrock K, Krumbholz M, Schönermarck U, Back W, Gross WL, Werb Z, et al. Netting neutrophils in autoimmune small-vessel vasculitis. Nature medicine. 2009;15(6):623-5.
5. Tomasson G, Grayson PC, Mahr AD, Lavalley M, Merkel PA. Value of ANCA measurements during remission to predict a relapse of ANCA-associated vasculitis--a meta-analysis. Rheumatology (Oxford). 2012;51(1):100-9.
6. van Dam LS, Dirikgil E, Bredewold EW, Ray A, Bakker JA, van Kooten C, et al. PR3-ANCAs predict relapses in ANCA-associated vasculitis patients after rituximab. Nephrol Dial Transplant. 2021;36(8):1408-17.
7. Berden AE, Ferrario F, Hagen EC, Jayne DR, Jennette JC, Joh K, et al. Histopathologic classification of ANCA-associated glomerulonephritis. Journal of the American Society of Nephrology : JASN. 2010;21(10):1628-36.
8. Hilhorst M, Wilde B, van Breda Vriesman P, van Paassen P, Cohen Tervaert JW. Estimating renal survival using the ANCA-associated GN classification. Journal of the American Society of Nephrology : JASN. 2013;24(9):1371-5.
9. Moroni G, Binda V, Leoni A, Raffiotta F, Quaglini S, Banfi G, et al. Predictors of renal survival in ANCA-associated vasculitis. Validation of a histopatological classification schema and review of the literature. Clinical and experimental rheumatology. 2015;33(2 Suppl 89):S-56-63.
10. Brix SR, Noriega M, Tennstedt P, Vettorazzi E, Busch M, Nitschke M, et al. Development and validation of a renal risk score in ANCA-associated glomerulonephritis. Kidney Int. 2018;94(6):1177-88.
11. Boudhabhay I, Delestre F, Coutance G, Gnemmi V, Quemeneur T, Vandenbussche C, et al. Reappraisal of Renal Arteritis in ANCA-associated Vasculitis: Clinical Characteristics, Pathology, and Outcome. J Am Soc Nephrol. 2021;32(9):2362-74.
12. Morris AD, Rowbottom AW, Martin FL, Woywodt A, Dhaygude AP. Biomarkers in ANCA-Associated Vasculitis: Potential Pitfalls and Future Prospects. Kidney360. 2021;2(3):586-97.
13. Moran SM, Scott J, Clarkson MR, Conlon N, Dunne J, Griffin MD, et al. The Clinical Application of Urine Soluble CD163 in ANCA-Associated Vasculitis. J Am Soc Nephrol. 2021;32(11):2920-32.
14. De Groot K, Rasmussen N, Bacon PA, Tervaert JW, Feighery C, Gregorini G, et al. Randomized trial of cyclophosphamide versus methotrexate for induction of remission in early systemic antineutrophil cytoplasmic antibody-associated vasculitis. Arthritis and rheumatism. 2005;52(8):2461-9.
15. Stone JH, Merkel PA, Spiera R, Seo P, Langford CA, Hoffman GS, et al. Rituximab versus cyclophosphamide for ANCA-associated vasculitis. The New England journal of medicine. 2010;363(3):221-32.
16. Jones RB, Tervaert JW, Hauser T, Luqmani R, Morgan MD, Peh CA, et al. Rituximab versus cyclophosphamide in ANCA-associated renal vasculitis. The New England journal of medicine. 2010;363(3):211-20.
17. Jayne DR, Gaskin G, Rasmussen N, Abramowicz D, Ferrario F, Guillevin L, et al. Randomized trial of plasma exchange or high-dosage methylprednisolone as adjunctive therapy for severe renal vasculitis. Journal of the American Society of Nephrology : JASN. 2007;18(7):2180-8.
18. Walsh M, Merkel PA, Peh CA, Szpirt WM, Puéchal X, Fujimoto S, et al. Plasma Exchange and Glucocorticoids in Severe ANCA-Associated Vasculitis. The New England journal of medicine. 2020;382(7):622-31.
19. Specks U, Merkel PA, Seo P, Spiera R, Langford CA, Hoffman GS, et al. Efficacy of remission-induction regimens for ANCA-associated vasculitis. The New England journal of medicine. 2013;369(5):417-27.
20. Pagnoux C, Quéméneur T, Ninet J, Diot E, Kyndt X, de Wazières B, et al. Treatment of systemic necrotizing vasculitides in patients aged sixty-five years or older: results of a multicenter, open-label, randomized controlled trial of corticosteroid and cyclophosphamide-based induction therapy. Arthritis Rheumatol. 2015;67(4):1117-27.
21. Jayne D, Rasmussen N, Andrassy K, Bacon P, Tervaert JW, Dadoniené J, et al. A randomized trial of maintenance therapy for vasculitis associated with antineutrophil cytoplasmic autoantibodies. The New England journal of medicine. 2003;349(1):36-44.
22. Etanercept plus standard therapy for Wegener's granulomatosis. The New England journal of medicine. 2005;352(4):351-61.
23. Gopaluni S, Smith RM, Lewin M, McAlear CA, Mynard K, Jones RB, et al. Rituximab versus azathioprine as therapy for maintenance of remission for anti-neutrophil cytoplasm antibody-associated vasculitis (RITAZAREM): study protocol for a randomized controlled trial. Trials. 2017;18(1):112.
24. Guillevin L, Pagnoux C, Karras A, Khouatra C, Aumaître O, Cohen P, et al. Rituximab versus azathioprine for maintenance in ANCA-associated vasculitis. The New England journal of medicine. 2014;371(19):1771-80.
25. Charles P, Terrier B, Perrodeau É, Cohen P, Faguer S, Huart A, et al. Comparison of individually tailored versus fixed-schedule rituximab regimen to maintain ANCA-associated vasculitis remission: results of a multicentre, randomised controlled, phase III trial (MAINRITSAN2). Annals of the rheumatic diseases. 2018;77(8):1143-9.

